Atopic dermatitis, innate immunity and infection
Published Web Location
https://doi.org/10.5070/D35hx776qpMain Content
Atopic dermatitis, innate immunity, and infection
Cristina Lopes1,2, Ana Filipa Duarte3, Osvaldo Correia1,3, Luís Delgado1,4,5
Dermatology Online Journal 17 (8): 4
1. Serviço e Laboratório de Imunologia Faculdade de Medicina, Universidade do Porto, Portugal2. Unidade de Imunoalergologia Hospital Pedro Hispano, Matosinhos, Portugal
3. Centro de Dermatologia Epidermis, Instituto CUF, Porto, Portugal
4 .Serviço de Patologia Clínica (Laboratório de Imunologia), Hospital São João, E.P.E., Porto, Portugal
5. CINTESIS (Centre for Research in Health Technologies and Information Systems), Faculdade de Medicina, Universidade do Porto, Portugal
Abstract
The prevalence of atopic dermatitis is increasing in western societies and this disease has a significant effect on the quality of life of patients and their families. The pathophysiology is complex, but there are recent insights on innate and adaptive immunity dysfunction in this condition that increases the predisposition to colonization/infection with characteristic types of microorganisms. We provide an up-to-date review of the pathophysiology of atopic dermatitis, highlighting the clinical implications of skin barrier dysfunction and immunological deregulation. We suggest a useful approach for handling exacerbations and infectious events.
Resumo
A prevalência da Dermatite atópica tem vindo a aumentar nas sociedades ocidentais com um impacto significativo na qualidade de vida dos doentes e das suas famílias. A sua patofisiologia é complexa com avanços recentes na compreensão da disfunção da imunidade inata e adaptativa e da maior predisposição para a colonização/infecção com tipos específicos de microrganismos. Este artigo faz uma revisão actualizada da patofisiologia da Dermatite atópica, focando as implicações clínicas da disfunção da barreira cutânea, desregulação imunológica e qual a melhor abordagem nas exacerbações e intercorrências infecciosas.
Introdução
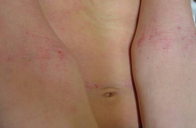 | 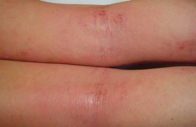 |
| Figure 1A | Figure 1B |
|---|
A Dermatite atópica (DA) é uma doença cutânea inflamatória crónica , recidivante, caracterizada por surtos e remissões de lesões intensamente pruriginosas e de localização variável [1]. A lesão típica da fase aguda consiste em erupção eritematosa, por vezes papulovesicular, exsudativa e com possível evolução para crosta. Na fase crónica as lesões tendem a ser descamativas, sem exsudados e por vezes com liquenificação (Figure 1). Na primeira infância a DA pode atingir toda a superfície corporal, mas geralmente poupa a região das fraldas; durante a segunda infância o atingimento da pele ocorre preferencialmente nos membros, particularmente nas superfícies flexoras. Na idade adulta, as lesões de dermatite predominam nas mãos e pés, superfície flexora dos membros e região cervical [1].
De acordo com o estudo ISAAC fase III, a prevalência global de sintomas de dermatite na faixa etária dos 6 aos 7 anos variou entre 0.9% na Índia e 22.5% no Equador e entre 0.2% na China e 24.6% na Colômbia, no grupo dos 13-14 anos, com os valores mais elevados em África e América Latina. Portugal apresentou valores de 9.3 % e 5.2%, respectivamente na faixa etária dos 6-7 e 13-14 anos [2].
A DA tem sido assim um problema major, tanto em países em vias de desenvolvimento como em países desenvolvidos [2], com um impacto significativo na qualidade de vida dos doentes e das suas famílias, e com um custo económico elevado [3].
Apesar do envolvimento frequente da resposta imune adaptativa na DA, através de mecanismos relacionados com a síntese de IgE, a sua patogénese não está completamente esclarecida mas a interacção com o ambiente, em indivíduos geneticamente predispostos, parece ser determinante [4].
Alterações na complexa interacção entre a barreira cutânea e o sistema imunológico inato e adaptativo têm vindo a ser progressivamente reconhecidas e parecem afectar quer o desenvolvimento, quer a gravidade da DA [5].
Nesta revisão abordamos a fisiopatologia da DA, com ênfase nas recentes descobertas que apontam para anomalias estruturais da epiderme e desregulação do sistema imunológico, bem como as suas potenciais implicações clínicas.
Imunidade Inata na Dermatite atópica
A pele é um dos mais importantes órgãos imunológicos. O sistema imunológico inato é filogeneticamente o mais antigo e é a primeira linha de defesa contra agressões do meio exterior. Inclui um conjunto heterogéneo de componentes que vão desde as barreiras físicas e químicas na pele e mucosas, a componentes celulares com actividade fagocítica, até a sistemas e mediadores que favorecem a resposta inflamatória à agressão [4]. Os elementos celulares da resposta imunológica inata têm capacidade de distinguir sequências únicas em certos patogénios e responder a esse reconhecimento. Este sistema reconhece os microrganismos através de um grupo de moléculas relativamente conservadas, os chamados receptores de reconhecimento de padrões (PRRs). Os PRRs incluem receptores transmembranares e intracelulares, tais como os os Toll-like receptors (TLRs), famílias de nucleotide –binding oligomeric domain (NOD), helicases, assim como moléculas solúveis no espaço intra e extravascular . A interacção dos PPRs com os seus ligandos leva a activação e recrutamento de células dendriticas, macrófagos, células NK e neutrófilos, resultando na produção de citocinas, quimiocinas e peptídeos antimicrobianos [6].
Verifica-se que os doentes com DA têm um risco aumentado de infecções por alguns tipos específicos de bactérias (Staphylococcus aureus ), vírus (herpes simples, pox vírus e papilomavírus humano) e fungos (Malassezia sympodialis). Esta susceptibilidade aumentada tem sido relacionada com possíveis deficiências do sistema imunológico inato em doentes com DA.
As células epiteliais da pele apresentam uma grande variedade de Toll like receptors (TLR) [7, 8]. Quando activadas produzem peptideos antimicrobianos incluindo defensinas, catelicidinas, dermicidina e psoriasina. Neste momento é consensual que a pele atópica tem níveis diminuídos de peptideos antimicrobianos, sendo o ambiente Th2, o predomínio de IL 10 ou ambos responsável por esta alteração [8].Um polimorfismo do gene de TLR 2 está associado a formas graves de DA com propensão para infecções bacterianas recorrentes, relacionadas com a sua disfunção [9](Tabela 1). O inibidor da calcineurina pimecrolimus, um imunomodulador tópico, aumenta a expressão in vitro de catelecidina, CD14 e B defensina 2 e 3 em resposta aos ligandos de TLR 2/6, com consequente inibição do crescimento do S. aureus [10].
É possível encontrar dois tipos de células dendriticas na pele lesada de doentes com DA: células miéloides e células plasmocitoides (em menor quantidade) [11]. As células de Langerhans e as células dendríticas epidérmicas inflamatórias pertencem ao grupo das células dendriticas mieloides exprimindo o receptor da alta afinidade para IgE(FcεRI) na pele lesada. Estas células têm um papel fundamental no uptake e apresentação de antigénios ou alergénios às células Th1/Th2 e muito provavelmente às células Treg [11]. Curiosamente é possível detectar a expressão de FcεRI na pele sã de doentes com DA durante períodos de exacerbação de outras manifestações de atopia como asma e rinite [11]. Parece haver evidência que as células de Langerhans têm um papel menos importante do que o incialmente esperado na iniciação e perpetuação da inflamação crónica e mais relevante na fase de sensibilização. De qualquer forma são relavantes no priming das células T naive num fenótipo Th2. Em contraste, a estimulação de FcεRI nas células dendriticas epidermicas inflamatórias leva a um switch para uma resposta Th1 e à libertação de grande quantidade de sinais pró-inflamatórios que contribuem para a amplificação da resposta alérgica [11].
As células dendriticas plasmocitoides, produzem grandes quantidades de IFN-α antivírico tipo I sendo também capazes de induzir respostas Th1 e Th2. São ricas em PPRs, incluindo TLR 7 e 9, produzindo grandes quantidades de IFNα quando activadas [12]. A pele de doentes com DA apresenta um menor número de células dendríticas plasmocitoides, quando comparada com a pele noutras patologias inflamatórias, como a psoríase, dermatite de contacto ou lúpus eritematoso sistémico [13]. Este deficit parcial parece também contribuir para a menor defesa da pele atópica perante a agressão microbiana quer bacteriana quer vírica [14].
Por outro lado, a atopia parece facilitar a adesão bacteriana, o primeiro passo na interacção microrganismo-hospedeiro. A IL-4, estimula a produção de fibronectina pelos fibroblastos cutâneos, servindo como âncora para moléculas da superfície bacteriana [15]. As citocinas Th-2 induzem uma menor expressão de filagrina através da inibição do seu factor de controlo - proteína A 11 ligadora de cálcio S100 (61/62)
Estas citocinas também interferem com o metabolismo lipidico suprimindo a produção de ceramida pelos queratinócitos [16].Globalmente, a polarização Th2 característica da doença alérgica resulta em alterações da barreira cutânea que promovem a entrada de microrganismos na pele.
É de notar que embora as citocinas mediadas por Th2 sejam importantes na fase aguda da DA, nas lesões crónicas verifica-se um aumento de IFN-γ e IL-12 características de um perfil Th1. A manutenção do processo inflamatório crónico envolve a produção de citocinas Th1 como IL-12 e IL-18 assim como de diversas citocinas associadas à remodelação como IL-11 e TGF beta 1 [11].
Os doentes com DA também apresentam alterações no recrutamento de neutrófilos, relacionados com a diminuição da IL 8, uma quimiocina CXC (CXCL8) quimiotáctica de neutrófilos [17], e com a produção de anticorpos IgE [18].
Assim, cada vez parece haver uma maior evidência de que a disfunção do sistema imunológico inato afecta de forma global o desenvolvimento e gravidade da DA (Tabela 2).
Disfunção da barreira cutânea
A integridade estrutural e funcional da barreira epitelial é um dos componentes primordiais do sistema de imunidade inata da pele e mucosas. A xerose cutânea, uma das características mais marcantes da dermatite atópica, é devida a um defeito da barreira cutânea com consequente a um aumento da perda de água transepidérmica. A função de barreira cutânea é assegurada pela acção conjunta de vários factores: proteínas do citoesqueleto de queratina (filagrina, involucrina e loricrina), lipideos intercelulares (ex ceramidas) provenientes de corpos lamelares derivados de queratinócitos, e diversas proteases epidérmicas como a enzima quimotriptica do estrato córneo. A filagrina (FLG) é uma proteína chave na diferenciação epidérmica servindo de template para a formação do invólucro córneo. Os seus produtos de degradação são fundamentais para o estrato córneo manter a capacidade de ligação à água.
Em 2006, a identificação de várias mutações do gene da filagrina em até 50% dos doentes com DA [19] renovou o interesse da comunidade científica pelos defeitos de barreira na DA. Diversos estudos demonstraram uma associação significativa entre mutações dos genes da FLG e o risco de DA persistente e grave e de início precoce [20]. Verificou-se no entanto, que um número significativo de doentes com DA não apresenta nenhuma das mutações conhecidas do gene da filagrina indiciando que outras proteínas da barreira cutânea para além da FLG estão envolvidas. Cerca de 40% dos doentes com alelos nulos para os genes da filagrina não têm DA [21] e muitos dos doentes com mutações do gene da FLG deixam de ter manifestações de DA ou têm períodos prolongados de remissão [22], sendo que mecanismos compensatórios devem ser activados de modo a restaurar o normal funcionamento da barreira cutânea. Paralelamente, os doentes com mutações deste gene têm maior risco de desenvolver asma mas apenas no contexto da presença da DA, reforçando a ligação clínica e imunopatológica das duas doenças e a possível relevância de uma barreira epitelial lesada para a sensibilização alérgica. [23]. Por outro lado, os doentes com um perfil Th2 de DA com alergia, asma e biomarcadores inflamatórios elevados como IgE sérica, linfopoietina do estroma tímico e quimiocinas com tropismo para linfócitos T, parecem ter doença cutânea mais vezes complicada por eczema herpeticum, Staphylococcus aureus ou infecções pelo vírus Molluscipox e papilomavirus humano [24], o que poderá representar uma outra face dessa disfunção da barreira cutânea.
Observações recentes de que os inibidores tópicos da calcineurina corrigem parcialmente o defeito de barreira cutânea nos doentes com DA e que a gentamicina pode recuperar a produção das cadeias de filagrina funcionais, demonstram a relação complexa existente entre a barreira cutânea a resposta imunológica na DA [25].
Dermatite atópica, microganismos e infecção
A pele humana é habitualmente colonizada por microrganismos não patogénicos. A flora microbiana está presente na superfície cutânea, no estrato córneo, no infundíbulo das glândulas sebáceas e nos folículos pilosos . A flora residente é composta por micrococos como estafilococos coagulase negativo, Peptococcus spp, Micrococcus spp, difteroides com corinebactérias e Brevibacterium spp, propionobacterias (infundíbulo das glândulas sebáceas) e bacilos gram negativos. O Pityrosporum ovale (Malassezia spp) está também habitualmente presente na pele.
A importância da flora cutânea residente na pele sã deriva do facto de gerar um sistema ecológico protector de patogénios. O Staphylococcus epidermidis, Propionobacterium acnes, corinebacteria e Pityrosporum ovale produzem lipases e estereases capazes de degradar os triglicerídeos em ácidos gordos livres diminuindo o pH da superfície cutânea impedindo o crescimento de outros microrganismos.
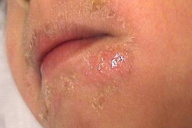 | 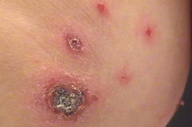 |
| Figure 2A | Figure 2B |
|---|
O Staphylococcus aureus (SA) coloniza a pele em situações específicas sendo sendo também responsável por infecções cutâneas, como impetigo (Figuras 2A and 2B) e formação de abcessos cutâneos.
Na DA, o SA pode ser cultivado em 90% das lesões cutâneas e pode colonizar pele aparentemente sã nestes doentes [26]. Este patogénio pode exacerbar ou contribuir para a inflamação cutânea persistente da DA pela secreção de toxinas com propriedades superantigénicas como a toxina 1 do síndrome do choque tóxico, enterotoxina estafilocócica B e C [27] levando à activação intensa de células T. A aplicação de enterotoxina B na pele pode induzir alterações eczematosas acompanhadas de infiltração de células T em resposta a este superantigénio [28]. Os doentes com DA podem produzir anticorpos IgE para as toxinas do SA presentes na pele, sendo que os basófilos destes doentes libertam histamina quando em contacto com a toxina relevante [29, 30].Este facto sugere que os superantigénios poderão induzir desgranulação mastocitária após penetrar a barreira cutânea, contribuindo para o prurido e inflamação agudas assim como perpetuando a inflamação crónica.
Os Staphylococcus aureus meticilino-resistentes (SAMR) têm emergido como um patogénio importante, evoluindo de uma causa de infecção nosocomial para infecção da comunidade [31]. Os SAMR invariavelmente produzem superantigénios tais como TSST-1, enterotoxina estafilocócica B e C. Wang et al identificaram uma nova classe de péptidos produzidos por SA, modulinas solúveis em fenol, que contribuem para a virulência aumentada de SAMR adquiridos na comunidade. Os doentes com DA parecem ser particularmente susceptíveis à colonização por estes agentes por serem frequentemente tratados com cursos de antibióticos anti-estafilocócicos . A possibilidade dos doentes com DA constituírem um reservatório importante destes patogenios na comunidade não está ainda bem estabelecida. [32].
 |  |
| Figure 2C | Figure 2D |
|---|
 |  |
| Figure 2E | Figure 2F |
|---|
Em cerca de 7 a 10% dos doentes com DA o curso clínico pode também ser complicado por infecções cutâneas víricas localizadas ou disseminadas, mais frequentemente por vírus herpes simplex (VHS) (Figura 2C), vírus papiloma humano (Figura 2D) ou vírus molluscipox (Figuras 2E and 2F) [14]. O eczema herpético é potencialmente fatal, e resulta de infecção disseminada por VHS tipo 1 e menos frequentemente tipo 2 [33].
Ocorre primariamente em doentes com DA parecendo estar associado a um fenótipo característico com polarização Th 2 (maior sensibilização a alergénios e história mais frequente de asma e alergia alimentar) [34]. Factores de risco para o eczema herpético incluem a DA de início precoce, grave ou não tratada, dermatite da cabeça e pescoço, infecções prévias por HSV e níveis séricos aumentados de IgE total com níveis elevados de IgE especificas, especialmente anti Malassezia sympodialis [35].
A disfunção da imunidade celular T parece também ser um factor predisponente para infecções víricas neste tipo de doentes. A disfunção de células T reguladoras cutâneas observada em doentes com DA [36], associa-se a uma resposta Th2-polarizada aos vírus, com uma menor resposta T-citotóxica. Por outro lado, num modelo experimental de eczema vacinatum, a produção de IL-17 e outras citocinas relacionadas com as células T reguladoras Th 17, reduzem a capacidade das células NK eliminarem células infectadas por vírus, promovendo a disseminação vírica e aumentando a susceptibilidade dos ratinhos com DA para o eczema vacinatum [37].
Implicações clínicas
O conceito de que a pele morfologicamente sã de doentes com DA não é normal em termos imunológicos, tem importantes implicações terapêuticas [38]. A ligação aumentada de Staphyloccocus aureus à pele na DA relaciona-se com a inflamação subjacente, mesmo que subclínica, e o tratamento com corticosteróides e inibidores tópicos da calcineurina diminui a colonização por SA [39]. Após um período de estabilização, os corticosteróides [40], mas sobretudo os inibidores da calcineurina tópicos, pela ausência dos efeitos secundários dos corticosteróides, podem ser aplicados de forma regular em áreas previamente envolvidas mas de aparência normal em vez de apenas serem aplicados no contexto de exacerbação (terapêutica pró-activa) [41].
Uma outra abordagem para diminuir a colonização por SA inclui a utilização de têxteis biofuncionais (Tabela 3). Este tipo de têxteis para além de garantirem o conforto adequado, e impedirem a perda transepidérmica de água, têm vindo a adquirir propriedades biologicamente activas. Estudos realizados com tecido impregnados com sais de prata reduziram a colonização estafilocócica (promovem o descolamento da membrana citoplasmática da parede celular), melhoraram parâmetros clínicos e reduziram a utilização de corticosteróides tópicos em doentes com DA [42, 43]. A utilização de tecidos com um tipo especial de seda permitiu uma diminuição significativa da gravidade da DA no grupo activo (SCORAD médio desceu de 43 para 30,p=0,003), em simultâneo a melhoria do score local da área coberta (de 32 para 19; p= 0,001) relativamente à área não coberta (de 31 para 26; p= 0,112) [44]. Novos tecidos impregnados com polímeros naturais com propriedades cicatrizantes e hidratantes da barreira cutânea, têm vindo a ser desenvolvidos nesta área com resultados promissores [45]. Recentemente foi avaliado o efeito in vitro de um biopolímero natural na proliferação e expressão de factores de virulência de SA derivados da pele de doentes com DA. Verificou-se que este biopolímero inibia não apenas a proliferação do SA, mas também a actividade da sua termonuclease, um marcador indirecto da produção de enterotoxinas. Estas observações permitem considerar que a utilização deste biopolímero em têxteis poderá vir a ser útil na abordagem de doentes com DA [46].
A possibilidade da presença de vírus herpes simplex como factor agravante da DA deve ser sempre considerada na presença de lesões vesiculares, muitas vezes confundidas com impetigo [47]. Na presença de vesiculas, erosões, por vezes com exsudado seroso ou sero-purulento, que não respondem a tratamento com antibiótico oral deve ser feita pesquisa de VHS por PCR, cultura de vírus, citodiagnóstico de Tzanck ou coloração Giemsa de células obtidas das vesículas. O tratamento é feito com aciclovir oral ou valaciclovir oral para infecções menos exuberantes, ou aciclovir parentérico em caso de doença disseminada [14].
Os fungos podem contribuir para a inflamação crónica nos doentes com DA. Anticorpos IgE para Malessezia sympodialis são encontrados mais frequentemente em doentes com dermatite da nuca e pescoço [48]. Mesmo estes doentes parecem responder melhor aos corticosteróides tópicos do que a anti-fúngicos tópicos e, por outro lado, a terapêutica anti-fúngica sistémica (itroconazol, cetoconazol ou fluconazole, em esquemas terapêuticos contínuos de 1 a 2 meses, seguidos de pulsos semanais nos casos intensos, recorrentes e em períodos de maior exacerbação) pode também beneficiar os doentes com DA através das suas propriedades anti-inflamatórias [49, 50].
Conclusões
• A Dermatite Atópica é uma patologia prevalente, associada à asma e sensibilização alérgica.
• A disfunção da barreira cutânea está bem exemplificada nos doentes com mutações do gene da filagrina, que têm DA de início mais precoce, mais grave, mais persistente e mais frequentemente associada a asma e sensibilização alérgica.
• A desregulação do sistema imunológico inato afecta o desenvolvimento e gravidade da DA, sendo a atopia um factor de agravamento neste processo. A redução de peptideos antimicrobianos, a desregulação dos receptores de reconhecimento de padrões, assim com a diminuição do recrutamento de células do sistema de imunidade inata para a pele, são algumas das possíveis explicações para a maior susceptibilidade perante certos microorganismos.
• A maioria dos doentes com DA estão colonizados por Staphylococcus aureus secretores de exotoxinas, mesmo em locais de pele aparentemente normal. Medidas anti-inflamatórias tópicas aplicadas de forma regular podem reduzir a colonização por Staphylococcus aureus e melhorar o controle da doença. Novas abordagens incluindo têxteis biofuncionais têm surgido como complementares na redução dessa colonização e no tratamento dos doentes com DA.
• A presença de vírus herpes simplex, como factor agravante da DA, deve ser sempre considerada na presença de lesões vesiculares. Os doentes com DA e mutações do gene da filagrina têm risco aumentado de ter eczema herpético.
Perspectivas futuras
Ficam ainda por esclarecer quais as proteínas que, para além da filagrina, são determinantes na manutenção da integridade da barreira cutânea e os mecanismos primordiais que levam a que, comparativamente a outras dermatoses inflamatórias, os doentes com DA apresentem maior propensão para colonização e infecção microbiana. No futuro será essencial determinar biomarcadores específicos da DA assim como estabelecer os seus fenótipos mais característicos.
Dada a complexidade patofisiológica da DA uma abordagem multifacetada dirigida à reparação e protecção da barreira cutânea, à redução da colonização microbiana e à desregulação imunológica, é essencial para uma maior eficácia terapêutica e melhoria da qualidade de vida destes doentes.
References
1. Eigenmann PA. Clinical features and diagnostic criteria of atopic dermatitis in relation to age. Pediatr Allergy Immunol. 2001;12 Suppl 14:69-74; [PubMed]2. Odhiambo JA, Williams HC, Clayton TO, Robertson CF, Asher MI. Global variations in prevalence of eczema symptoms in children from ISAAC Phase Three. J Allergy Clin Immunol. 2009 Dec;124(6):1251-8 e23; [PubMed]
3. Akdis CA, Akdis M, Bieber T, Bindslev-Jensen C, Boguniewicz M, Eigenmann P, et al. Diagnosis and treatment of atopic dermatitis in children and adults: European Academy of Allergology and Clinical Immunology/American Academy of Allergy, Asthma and Immunology/PRACTALL Consensus Report. Allergy. 2006 Aug;61(8):969-87; [PubMed]
4. Cork MJ, Danby SG, Vasilopoulos Y, Hadgraft J, Lane ME, Moustafa M, et al. Epidermal barrier dysfunction in atopic dermatitis. J Invest Dermatol. 2009 Aug;129(8):1892-908; [PubMed]
5. De Benedetto A, Agnihothri R, McGirt LY, Bankova LG, Beck LA. Atopic dermatitis: a disease caused by innate immune defects? J Invest Dermatol. 2009 Jan;129(1):14-30; [PubMed]
6. Janeway CA Jr MR. Innate immune recognition. Annu Rev Immunol. 2002;20:197-216; [PubMed]
7. Schauber J, Gallo RL. Antimicrobial peptides and the skin immune defense system. J Allergy Clin Immunol. 2009 Sep;124(3 Suppl 2):R13-8; [PubMed]
8. Ong PY, Ohtake T, Brandt C, Strickland I, Boguniewicz M, Ganz T, et al. Endogenous antimicrobial peptides and skin infections in atopic dermatitis. N Engl J Med. 2002 Oct 10;347(15):1151-60; [PubMed]
9. Mrabet-Dahbi S DA NM, Frey M, Draing C, Brand S, et al. The toll-like receptor 2 R753Q mutation modifies cytokine production and Toll-like receptor expression in atopic dermatitis. J Allergy Clin Immunol 2008 (12):1013-19; ; [PubMed]
10. Buchau AS SJ, Hultsch T, Stuetz A, Gallo RL. . Pimecrolimus enhances TLR2/6-induced expression of antimicrobial peptides in keratinocytes. J Invest Dermatol 2008;128:2646-54; [PubMed]
11. Novak N, Koch S, Allam JP, Bieber T. Dendritic cells: bridging innate and adaptive immunity in atopic dermatitis. J Allergy Clin Immunol. 2010 Jan;125(1):50-9; [PubMed]
12. Cao W LY. Innate immune functions of plasmacytoid dendritic cells. Curr Opin Immunol 2007;19(24-30.) [PubMed]
13. Stary G BC, Stingl G, Kopp T. Dendritic cells in atopic dermatitis: expression of FcepsilonRI on two distinct inflammation-associated subsets. Int Arch Allergy Immunol. 2005;138:278-90; [PubMed]
14. Wollenberg A, Wetzel S, Burgdorf WH, Haas J. Viral infections in atopic dermatitis: pathogenic aspects and clinical management. J Allergy Clin Immunol. 2003 Oct;112(4):667-74; [PubMed]
15. Postlethwaite AE HM, Katai H, Raghow R. . Human fibroblasts synthesize elevated levels of extracellular matrix proteins in response to interleukin 4. J Clin Invest 1992;90:1479-85; [PubMed]
16. Miscke D KB, Marenholz I, Volz A, Ziegler A. . Genes encoding structural proteins of epidermal cornification and S100 calcium-binding proteins form a gene complex on human chromosome 1q21. J Invest Dermatol. 1996;106:989-92; [PubMed]
17. Nomura I GE, Howell MD, Hamid QA, Ong PY, Hall CF et al. Cytokine milieu of atopic dermatitis, as compared to psoriasis skin prevents induction of innate immune response genes. J Immunol 2003;171:3262-9.; [PubMed]
18. al-Mohanna F PR, Kawaasi A. Inhibition of neutrophil functions by human immunoglobulin E. J Allergy Clin Immunol. 1993;92(757-66) [PubMed]
19. Palmer CN IA, Terron-Kwiatkowski A, Zhao Y, Liao H, Lee SP, et al. Common loss-of-function variants of the epidermal barrier protein filaggrin are a major predisposing factor for atopic dermatitis. Nat Genet 2006(38):441-6; [PubMed]
20. Rodriguez E, Baurecht H, Herberich E, Wagenpfeil S, Brown SJ, Cordell HJ, et al. Meta-analysis of filaggrin polymorphisms in eczema and asthma: robust risk factors in atopic disease. J Allergy Clin Immunol. 2009 Jun;123(6):1361-70 e7; [PubMed]
21. O’Regan GM SA, McLean WH, Irvine AD. Filaggrin in atopic dermatitis. J Allergy Clin Immunol 2008;122:689-93; [PubMed]
22. Henderson J NK. The burden of disease associated with filaggrin mutations: a population-based, longitudinal birth cohort study. J Allergy Clin Immunol 2008;121:872-7; [PubMed]
23. McLean WH, Palmer CN, Henderson J, Kabesch M, Weidinger S, Irvine AD. Filaggrin variants confer susceptibility to asthma. J Allergy Clin Immunol. 2008 May;121(5):1294-5; author reply 5-6; [PubMed]
24. Beck LA BM, Hata T, Schneider LC, Hanifin J, Gallo R, et al. . Phenotype of atopic dermatitis subjects with a history of eczema herpeticum. J Allergy Clin Immunol 2009;124:260; [PubMed]
25. Jung T SG. Atopic dermatitis: therapeutic concepts evolving from new pathophysiologic insights. J Allergy Clin Immunol. 2008;122:1074-81; [PubMed]
26. Cho SH, Strickland I, Boguniewicz M, Leung DY. Fibronectin and fibrinogen contribute to the enhanced binding of Staphylococcus aureus to atopic skin. J Allergy Clin Immunol. 2001 Aug;108(2):269-74; [PubMed]
27. Schlievert PM, Case LC, Strandberg KL, Abrams BB, Leung DY. Superantigen profile of Staphylococcus aureus isolates from patients with steroid-resistant atopic dermatitis. Clin Infect Dis. 2008 May 15;46(10):1562-7; [PubMed]
28. Skov L, Olsen JV, Giorno R, Schlievert PM, Baadsgaard O, Leung DY. Application of Staphylococcal enterotoxin B on normal and atopic skin induces up-regulation of T cells by a superantigen-mediated mechanism. J Allergy Clin Immunol. 2000 Apr;105(4):820-6; [PubMed]
29. Leung DY, Harbeck R, Bina P, Reiser RF, Yang E, Norris DA, et al. Presence of IgE antibodies to staphylococcal exotoxins on the skin of patients with atopic dermatitis. Evidence for a new group of allergens. J Clin Invest. 1993 Sep;92(3):1374-80; [PubMed]
30. Bunikowski R, Mielke ME, Skarabis H, Worm M, Anagnostopoulos I, Kolde G, et al. Evidence for a disease-promoting effect of Staphylococcus aureus-derived exotoxins in atopic dermatitis. J Allergy Clin Immunol. 2000 Apr;105(4):814-9; [PubMed]
31. Schlievert PM, Strandberg KL, Lin YC, Peterson ML, Leung DY. Secreted virulence factor comparison between methicillin-resistant and methicillin-sensitive Staphylococcus aureus, and its relevance to atopic dermatitis. J Allergy Clin Immunol. 2010 Jan;125(1):39-49; [PubMed]
32. Boguniewicz M, Sampson H, Leung SB, Harbeck R, Leung DY. Effects of cefuroxime axetil on Staphylococcus aureus colonization and superantigen production in atopic dermatitis. J Allergy Clin Immunol. 2001 Oct;108(4):651-2; [PubMed]
33. Peng WM JC, Bussmann C, Bogdanow M, Hart J, Leung DY, et al. . Risk factors of atopic dermatitis patients for eczema herpeticum. J Invest Dermatol. 2007;127:1261-3; [PubMed]
34. Gao PS, Rafaels NM, Hand T, Murray T, Boguniewicz M, Hata T, et al. Filaggrin mutations that confer risk of atopic dermatitis confer greater risk for eczema herpeticum. J Allergy Clin Immunol. 2009 Sep;124(3):507-13, 13 e1-7; [PubMed]
35. Wollenberg A ZC, Wetzel S, Plewig G, Przybilla B. . Predisposing factors and clinical features of eczema herpeticum: a retrospective analysis of 100 cases. J Am Acad Dermatol. 2003;49:198-205; [PubMed]
36. Freyschmidt EJ, Mathias CB, Diaz N, MacArthur DH, Laouar A, Manjunath N, et al. Skin inflammation arising from cutaneous regulatory T cell deficiency leads to impaired viral immune responses. J Immunol. 2010 Jul 15;185(2):1295-302; [PubMed]
37. von Bubnoff D, Andres E, Hentges F, Bieber T, Michel T, Zimmer J. Natural killer cells in atopic and autoimmune diseases of the skin. J Allergy Clin Immunol. 2010 Jan;125(1):60-8; [PubMed]
38. Hamid Q, Boguniewicz M, Leung DY. Differential in situ cytokine gene expression in acute versus chronic atopic dermatitis. J Clin Invest. 1994 Aug;94(2):870-6; [PubMed]
39. Hung SH LY, Chu CY, Lee CC, Liang TC, Yang YH, et al. . Staphylococcus colonization in atopic dermatitis treated with fluticasone or tacrolimus with or without antibiotics. Ann Allergy Asthma Immunol. 2007;98:51-6; [PubMed]
40. Berth-Jones J DR, Golsch S, Livden JK, Van Hooteghem O, Allegra F,, al. e. Twice weekly fluticasone propionate added to emollient maintenance treatment to reduce risk of relapse in atopic dermatitis: randomised, double blind, parallel group study. BMJ 2003;326:1367; [PubMed]
41. Wollenberg A, Bieber T. Proactive therapy of atopic dermatitis--an emerging concept. Allergy. 2009 Feb;64(2):276-8; [PubMed]
42. Gauger A. Silver-coated textiles in the therapy of atopic eczema. Curr Probl Dermatol. 2006;33:152-64; [PubMed]
43. Gauger A, Fischer S, Mempel M, Schaefer T, Foelster-Holst R, Abeck D, et al. Efficacy and functionality of silver-coated textiles in patients with atopic eczema. J Eur Acad Dermatol Venereol. 2006 May;20(5):534-41; [PubMed]
44. Ricci G PA. Clinical effectivenes of a silk fabric in the treatment of atopic dermatitis,. Br J Dermatol 2004;150:127-31; [PubMed]
45. Fernandes JC, Freni K. Tavaria, Susana C. Fonseca, Óscar S. Ramos, Manuela E. Pintado, and F. Xavier Malcata. In Vitro Screening for Antimicrobial Activity of Chitosans and Chitooligosaccharides, Aiming at Potential Uses in Functional Textiles. J Microbiol Biotechnol 2010;20(2):311-8; [PubMed]
46. Tavaria FL, C; Soares, J; Pintado, M;, Delgado L. Allergy 65 (Suppl 92): 209-682.
47. Bork K BW. Increasing incidence of eczema herpeticum: analysis of seventy-five cases. J Am Acad Dermatol 1988(19):1024-9; [PubMed]
48. Boguniewicz M, Schmid-Grendelmeier P, Leung DY. Clinical pearls: atopic dermatitis. J Allergy Clin Immunol. 2006 Jul;118(1):40-3; [PubMed]
49. Darabi K HS, Bechtel MA, Zirwas M. The role of Malassezia in atopic dermatitis affecting the head and neck of adults. J Am Acad Dermatol. 2009(60) [PubMed]
50. AF N. Framing the future of antifungals in atopic dermatitis. Dermatology. 2003 2003;206(4) [PubMed]
© 2011 Dermatology Online Journal

